Grafit, molekyleformel: C, molekylvægt: 12,01, er en form for grundstof kulstof, hvert kulstofatom er forbundet med tre andre kulstofatomer (arrangeret i bikage-sekskanter) for at danne et kovalent molekyle. Fordi hvert kulstofatom udsender en elektron, dem der kan bevæge sig frit, så grafit er en leder.
Grafit er et af de blødeste mineraler, og dets anvendelser omfatter fremstilling af blyanter og smøremidler. Kulstof er et ikke-metallisk grundstof placeret i anden cyklus IVA-gruppe i det periodiske system. Grafit dannes ved høje temperaturer.
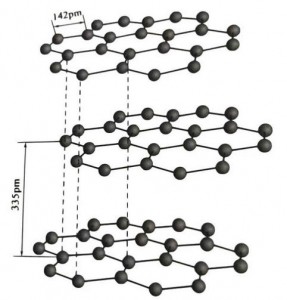
Grafit er et krystallinsk mineral af kulstofelementer, og dets krystallinske gitter er en sekskantet lagdelt struktur. Afstanden mellem hvert maskelag er 3,35A, og afstanden mellem carbonatomer i det samme maskelag er 1,42A. Det er et sekskantet krystalsystem med en komplet lagdelt spaltning. Spaltningsoverfladen er hovedsageligt molekylære bindinger, mindre attraktive for molekyler, så dens naturlige flyder er meget god.
I grafitkrystaller danner carbonatomerne i samme lag en kovalent binding med sp2-hybridisering, og hvert carbonatom er forbundet med tre andre atomer i tre kovalente bindinger. De seks carbonatomer danner en seks-kontinuerlig ring i samme plan, der strækker sig ind i en lamelstruktur, hvor bindingslængden af CC-bindingen er 142pm, hvilket er nøjagtigt inden for bindingslængdeområdet for atomkrystallen, altså for det samme lag , det er en atomisk krystal. Kulstofatomer i samme plan har en p-bane, som overlapper hinanden. Elektroner er relativt frie, svarende til frie elektroner i metaller, så grafit kan lede varme og elektricitet, hvilket er karakteristisk for metalkrystaller. Således også klassificeret som metalliske krystaller.
Mellemlaget af grafitkrystal er adskilt af 335pm, og afstanden er stor. Det er kombineret med van der Waals kraft, det vil sige, at laget tilhører den molekylære krystal. Men fordi bindingen af carbonatomer i det samme plane lag er meget stærk og ekstremt svær at ødelægge, er opløsningspunktet for grafit også meget højt, og dets kemiske egenskaber er stabile.
I lyset af dens specielle bindingstilstand, kan den ikke betragtes som en enkelt krystal eller polykrystal, er grafit nu generelt betragtet som en blandet krystal.
Indlægstid: 31-jul-2023